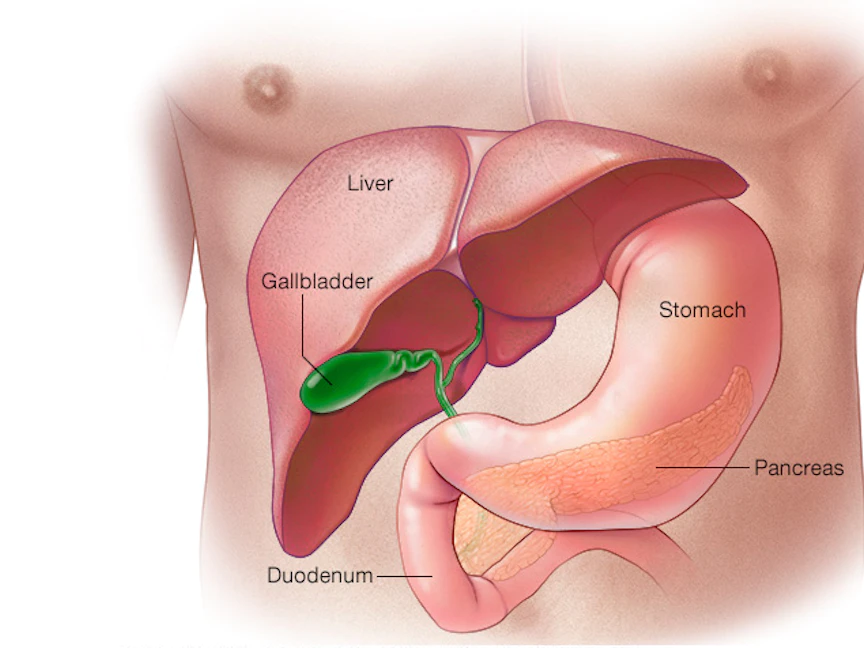
يعد سرطان البنكرياس أحد أكثر أنواع السرطان فتكاً. فبعد التشخيص، يعيش أقل من 10% من المرضى لمدة خمس سنوات.
وفي حين أن بعض العلاجات الكيميائية فعالة في البداية، غالباً ما تصبح أورام البنكرياس مقاومة لها، كما ثبت أيضاً صعوبة علاج المرض باستخدام الأساليب الأحدث مثل العلاج المناعي.
إلا أن فريق "معهد ماساتشوستس للتكنولوجيا" تمكن من تطوير استراتيجية جديدة للعلاج المناعي يُمكنها القضاء على أورام البنكرياس في الفئران، حسبما جاء في دراسة منشورة في دورية "كانسر سيل".
مزيج من الأدوية المناعية
ومن المتوقع أن يدخل العلاج الجديد، وهو مزيج من ثلاثة أدوية تساعد في تعزيز دفاعات الجسم المناعية ضد الأورام، في التجارب السريرية في وقت لاحق من هذا العام.
لا توجد الكثير من الخيارات العلاجية الجيدة لسرطان البنكرياس. فإذا ما أدى هذ النهج إلى استجابات فعالة لدى المرضى، فسيكون له تأثير كبير في المُصابين بذلك النوع من الأورام.
ويمتلك الجهاز المناعي نظام مبكر للتعرف على الخلايا السرطانية. إذ يحتوي على مجموعة من الخلايا المناعية التائية التي تتعرف إلى البروتينات التي تُفرزها الأورام السرطانية.
في الحالات الطبيعية، تقوم المناعة بتدمير الأورام بشكل كامل. لكن، وحين تتمكن الخلايا الورمية من خلق بيئة مُثبطة للمناعة، تقوم "بفرملة" الجهاز المناعي، فتفشل الخلايا التائية في التعرف إلى البروتينات السرطانية ولا تقوم بمهاجمة الورم، ما يساعده على البقاء والتوغل في الجسم.
نقاط التفتيش
يعمل العلاج المناعي الأكثر شيوعاً عن طريق استخدام ما يُعرف باسم نقاط التفتيش والتي تزيل الفرامل عن هذه الخلايا التائية، وتجددها للتمكن من تدمير الأورام.
وتستهدف فئة واحدة من أدوية العلاج المناعي التي أثبتت نجاحاً في علاج العديد من أنواع السرطان، التفاعلات بين بروتين يُسمى PD-L1، وهو بروتين مرتبط بالسرطان يعمل على إيقاف الخلايا التائية، وPD-1، وهو بروتين الخلية التائية الذي يرتبط به PD-L1.
وتمت الموافقة على الأدوية التي تمنع PD-L1 أو PD-1، والتي تسمى أيضاً مثبطات نقطة التفتيش، لعلاج السرطانات مثل سرطان الجلد وسرطان الرئة، لكن تأثيرها ضئيل جداً في أورام البنكرياس.
افترض بعض الباحثين، أن هذا الفشل يرجع إلى أن أورام البنكرياس لا تفرز العديد من البروتينات السرطانية. وهو أمر من شأنه أن يعطي الخلايا التائية أهدافاً أقل للهجوم، لذا حتى عند تحفيز الخلايا التائية بواسطة مثبطات نقاط التفتيش، فإنها لن تكون قادرة على تحديد الخلايا السرطانية وتدميرها.
بروتينات مختلفة
لكن بعض الدراسات الحديثة أظهرت أن العديد من أورام البنكرياس تفرز في الواقع البروتينات الخاصة بالأورام السرطانية. قاد هذا الاكتشاف الباحثين إلى الشك في أن نوعاً مختلفاً من الفرامل، بخلاف نظام PD-1 / PD-L1 يعطل الخلايا التائية في مرضى سرطان البنكرياس.
في دراسة باستخدام نماذج الفئران لسرطان البنكرياس، وجد الباحثون أنه في الواقع، لا يتم التعبير عن PD-L1 بشكل كبير في خلايا سرطان البنكرياس. بدلاً من ذلك، تُظهر معظم خلايا سرطان البنكرياس بروتيناً يسمى CD155، والذي ينشط مستقبلاً على الخلايا التائية يعرف باسم TIGIT.
عند يتم تنشيط TIGIT، تدخل الخلايا التائية حالة تعرف باسم "استنفاد الخلايا التائية" فلا تستطيع شن هجوم على الخلايا السرطانية في البنكرياس.
في تحليل للأورام التي تمت إزالتها من مرضى سرطان البنكرياس، لاحظ الباحثون إفراز كمية كبيرة من مستقبل TIGIT والذي يُدمر الخلايا التائية في نحو 60% من المرضى، ووجدوا أيضاً مستويات عالية من بروتين CD155 على الخلايا السرطانية من المرضى، وتأكد الباحثون أن تلك الآلية هي ما تجعل أورام البنكرياس مُقاومة للعلاج.
ثم انطلق الباحثون لمعرفة ما إذا كان بإمكانهم استخدام هذه المعرفة لتجديد الخلايا التائية المنهكة وتحفيزها على مهاجمة الخلايا السرطانية في البنكرياس. فقاموا باختبار مجموعة متنوعة من الأدوية التجريبية التي تثبط PD-1 وTIGIT جنباً إلى جنب مع نوع آخر من الأدوية يسمى بمُعزز الأجسام المضادة CD40.
والأجسام المضادة لـ CD40 -والتي يتم حالياً تقييم بعضها سريرياً لعلاج سرطان البنكرياس- هي عقاقير تنشط الخلايا التائية، وتدفعها إلى الأورام.
وقف نمو السرطان
وفي الاختبارات التي أجريت على الفئران، وجد فريق "معهد ماساتشوستس للتكنولوجيا"، أن الأدوية المضادة لـ PD-1 كان لها تأثير ضئيل من تلقاء نفسها، كما هو موضح سابقاً لسرطان البنكرياس. ووجدوا أيضاً أن الجسم المضاد الناشط CD40 جنباً إلى جنب مع مثبط PD-1 أو مثبط TIGIT، كان قادراً على وقف نمو الورم في بعض الحيوانات، لكنه لم يقلص الأورام بشكل كبير.
لكن، وعندما قاموا بدمج الأجسام المضادة CD40 مع كل من مثبط PD-1 ومثبط TIGIT، وجدوا تأثيراً كبيراً. فقد تقلصت أورام البنكرياس في نحو نصف الحيوانات التي خضعت لهذا العلاج، وفي 25% من الفئران، اختفت الأورام تماماً.
فضلاً عن ذلك، لم تنمُ الأورام مرة أخرى بعد توقف العلاج.
ويُخطط فريق البحث لبدء تجربة سريرية على البشر في القريب العاجل. كما يخطط أيضاً في إجراء مجموعة من التحاليل على أنواع أورام البنكرياس لمعرفة أيهم سيكون أفضل في الاستجابة للدواء الجديد.




