كشفت دراسة حديثة أن هياكل لزجة تفرزها خلايا مناعية، تعرف بـ"الشباك خارج الخلوية"، تلعب دوراً محورياً في تطور حالة مرضية معطلة تسمى "التعظم غير المتجانس".
في هذه الحالة، تنمو عظام في أماكن لا ينبغي أن توجد فيها، وتُظهر النتائج أن استهداف هذه الشباك بأدوية متاحة، أو تجريبية قد يحد من تقدم المرض.
تجمع الدراسة، التي نُشرت ضمن أبحاث American Association for the Advancement of Science، بين نماذج حيوانية وعينات بشرية، مقدمة دليلاً قوياً على أن آلية مناعية معروفة بمقاومة العدوى قد تتحول، في ظروف معينة، إلى محرك لتكون عظام شاذة داخل الأنسجة الرخوة.
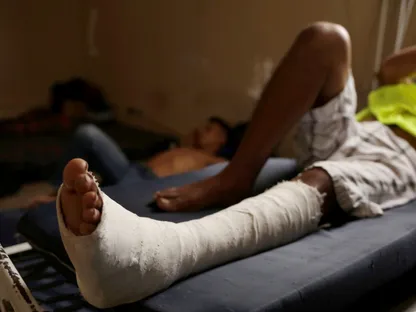
والتعظم غير المتجانس هو اضطراب يحدث عندما تتكون عظام حميدة في أنسجة رخوة، مثل العضلات والجلد ومحافظ المفاصل؛ وغالباً ما يظهر بعد إصابات العضلات والعظام، أو عقب جراحات استبدال المفاصل، وخاصة في منطقة المرفق، وقد يتفاقم تدريجياً.
الخلايا النخاعية
رغم أن النمو العظمي في هذه الحالة ليس سرطانياً، إلا أن تأثيره قد يكون شديداً؛ إذ يسبب ألماً حاداً وتيبساً، وقد ينتهي بفقدان كامل لوظيفة المفصل، بل وإصابة الأعصاب.
ولا تزال خيارات العلاج الحالية محدودة؛ جراحات استئصال عالية المخاطر، أو أدوية بفعالية سريرية محدودة.
وركزت الدراسة الجديدة على نوع من الخلايا المناعية يعرف بالخلايا النخاعية، وهي من أوائل الخلايا التي تصل إلى موقع الإصابة؛ هذه الخلايا تطلق عادة "شباكاً خارج خلوية"، وهي هياكل شبيهة بالشبكات، تتكون من الحمض النووي وبروتينات، لتطويق الميكروبات والقضاء عليها.
لكن الباحثين اكتشفوا أن هذه الشباك قد تؤدي دوراً غير متوقع؛ ففي تحليل لعينات من 20 مريضاً يعانون التعظم غير المتجانس، وجدت كميات مرتفعة من هذه الشباك داخل مواضع الآفات، ما يشير إلى ارتباط وثيق بين نشاطها، وتكون العظام الشاذة، أي أن ما صمم ليكون "فخاً للبكتيريا" قد يتحول في بيئة الإصابة إلى "قالب" يحفز تكوين عظام في المكان الخطأ.
وللتأكد من هذا الدور، لجأ الباحثون إلى نماذج الفئران، وعطلوا جينين أساسيين يطلق عليهما DNase1 وDNase1l3، وهما مسؤولان عن تفكيك هذه الشباك والتخلص منها.
وقال الباحثون إن الفئران التي افتقرت إلى هذين الجينين شهدت تفاقماً ملحوظاً في التعظم غير المتجانس، ما يدل على أن تراكم الشباك خارج الخلوية يسرع تطور المرض.
في المقابل، عندما استنزف الباحثون الخلايا النخاعية نفسها، أي المصدر الرئيسي لهذه الشباك، انخفضت شدة الحالة، ما يعزز الفرضية القائلة إن هذه الهياكل تلعب دوراً سببياً، وليس مجرد علامة مصاحبة.
علاج نمو العظام الشاذة
واختبر الباحثون دواءً معتمداً من منظمة الغذاء والدواء الأميركية (FDA) يعرف باسم Dornase alfa، والمستخدم بالفعل في أمراض أخرى لتفكيك الحمض النووي خارج الخلايا، إلى جانب مركب تجريبي يدعى GSK484.
وأظهرت النتائج أن العلاجين نجحا في تقليل تكون الشباك خارج الخلوية، ما انعكس بدوره على انخفاض واضح في نمو العظام الشاذة لدى الفئران، والأهم، كما يقول الباحثون، أن هذا التأثير لم يأت على حساب نمو العظام الطبيعي، وهو عامل حاسم في تقييم أي علاج محتمل.
وتفتح هذه النتائج الباب أمام إعادة توظيف أدوية موجودة بالفعل، وهو مسار غالباً ما يكون أسرع في الوصول إلى الاستخدام السريري مقارنة بتطوير أدوية جديدة من الصفر.
ويرى الباحثون أن الشباك خارج الخلوية قد تخلق بيئة موضعية تحفز الخلايا الجذعية، أو الخلايا المكونة للعظام على التمايز في اتجاه غير طبيعي، كما قد تسهم في إطلاق إشارات التهابية تعزز هذه العملية.
وبحسب تفسيرهم، فإن مراقبة أو تقليل هذه الشباك قد يوقف "سلسلة الأحداث" التي تبدأ بالالتهاب، وتنتهي بتكون عظام غير مرغوب فيها.
وإذا تأكدت هذه النتائج في تجارب سريرية على البشر، فقد يصبح من الممكن تطوير علاج يستهدف آلية محددة بدقة، بدلاً من الاعتماد على تدخلات جراحية أو أدوية عامة التأثير.
وتسلط الدراسة الضوء على جانب أوسع؛ فكيف يمكن لآليات مناعية أساسية، مصممة لحماية الإنسان، أن تتحول إلى عوامل مرضية في سياقات معينة، وهو مفهوم يزداد حضوره في أبحاث الأمراض الالتهابية والمناعية.
لكن رغم قوة النتائج، إلا أن الباحثين حذروا من التسرع في تطبيقها سريرياً؛ فالشباك خارج الخلوية تلعب دوراً مهماً في مكافحة العدوى، ما يعني أن تثبيطها قد يعرض المرضى لخطر أكبر من الالتهابات.
كما أن معظم البيانات جاءت من نماذج حيوانية، إلى جانب عدد محدود نسبياً من عينات المرضى، ما يستدعي إجراء دراسات أوسع لتأكيد الفعالية والأمان.