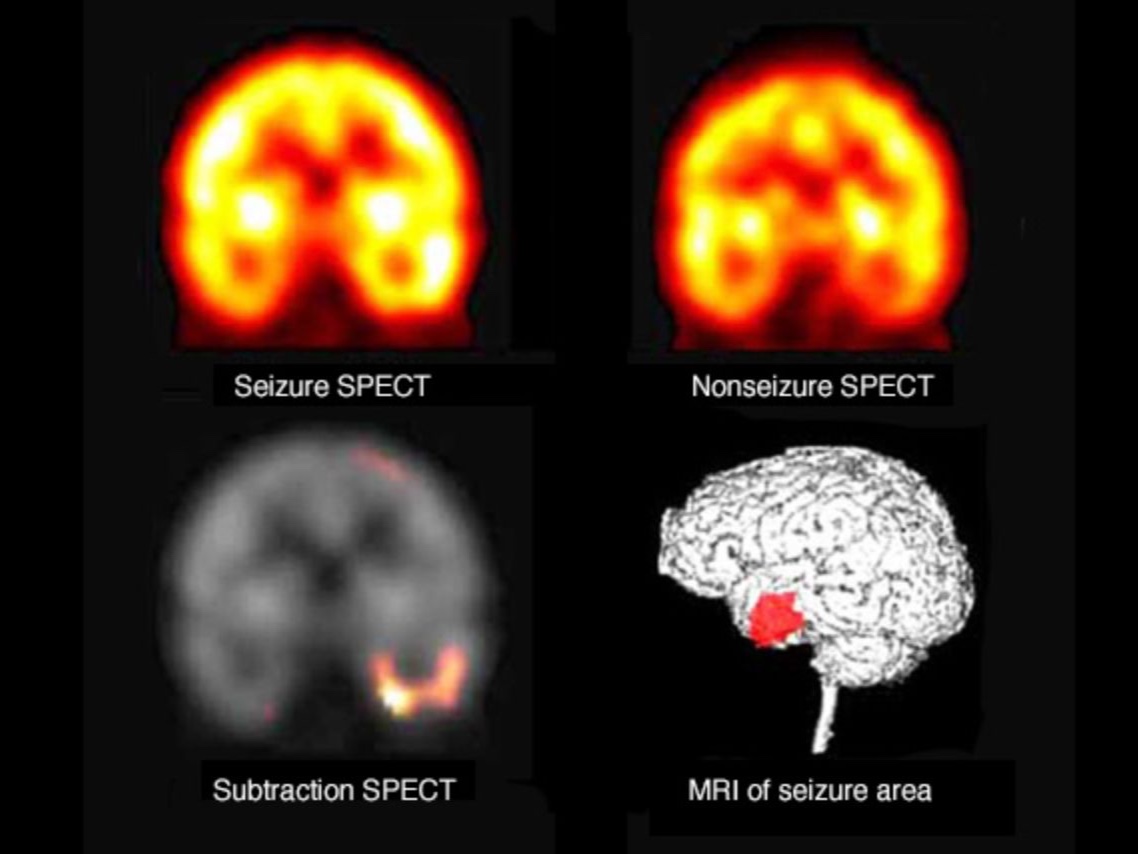
أظهرت تجارب سريرية مبكرة لعلاج يعتمد على تنظيم الجينات نتائج واعدة في علاج أحد أخطر أشكال الصرع الوراثي، إذ نجح العلاج الجديد في تقليل نوبات الصرع بشكل كبير وتحسين عدد من الأعراض العصبية والتطورية لدى الأطفال المصابين بمتلازمة "درافيت".
وتعد هذه التجارب الأولى من نوعها التي تستهدف السبب الجيني المباشر لهذا المرض، ما يمثل خطوة مهمة في تطوير علاجات أكثر دقة لأمراض الجهاز العصبي.
النتائج التي نُشرت في مجلة New England Journal of Medicine جاءت من تجربتين سريريتين من المرحلتين الأولى والثانية المبكرة من مستشفى "آن وروبرت إتش لوري" للأطفال في شيكاجو، أحد أبرز المراكز المتخصصة في طب الأطفال وأبحاث الأعصاب في الولايات المتحدة.
وأظهرت النتائج أن العلاج الجيني الجديد آمن ويمكن للمرضى تحمله، خاصة لدى الأطفال المصابين بمتلازمة "درافيت" الذين لا تستجيب حالتهم للأدوية التقليدية المضادة للنوبات.
اضطراب نادر
وتعد متلازمة درافيت اضطراباً عصبياً وراثياً نادراً يظهر عادة في مرحلة الطفولة المبكرة ويتطور مع الوقت. ويعاني معظم المرضى من مجموعة واسعة من الأعراض تشمل ضعف القدرات المعرفية وصعوبات التواصل واضطرابات سلوكية ومشكلات في الحركة وتأخر النمو إضافة إلى سمات مرتبطة باضطراب طيف التوحد. كما يواجه العديد منهم صعوبات في التغذية وضعف الشهية وفقدان الوزن.
وقالت المؤلفة المشاركة في الدراسة ليندا لوكس، رئيسة مركز الصرع بمستشفى لوري للأطفال والأستاذة المشاركة في طب الأطفال بكلية فاينبرج للطب بجامعة "نورثويسترن" (Northwestern University): "نتائجنا واعدة للغاية، خاصة أنه لا توجد حالياً أي علاجات معتمدة تستهدف السبب الأساسي لمتلازمة درافيت".
وأضافت أن هذا العلاج يستهدف الجذر الجيني الحقيقي للمرض "فقد لاحظنا تحسناً في أعراض النمو والوظائف المعرفية إلى جانب السيطرة على النوبات، وهو أمر غير مسبوق".
وتقول الدراسة إن المرض بطفرة في جين يسمى SCN1A المسؤول عن إنتاج جزء مهم من مستقبلات قنوات الصوديوم في الخلايا العصبية. ويوضح الباحثون أن المرضى يمتلكون نسخة متحورة من هذا الجين إلى جانب نسخة سليمة، لكن الطفرة تؤدي إلى ما يعرف بنقص التعبير الجيني، أي أن الجسم ينتج نصف الكمية الطبيعية فقط من البروتين الضروري لوظيفة الخلايا العصبية. ويؤدي هذا الخلل إلى حدوث نوبات الصرع إضافة إلى اضطرابات معرفية وحركية.
طريقة مختلفة
العلاج الجديد، الذي يحمل اسم "زوريفونسيرسن" يعمل بطريقة مختلفة عن العلاجات التقليدية، إذ يستهدف النسخة السليمة من الجين SCN1A ويحفزها للعمل بكفاءة أعلى لتعويض النقص الناتج عن النسخة المتحورة. ويتم إعطاء العلاج عن طريق حقنه في السائل النخاعي من خلال إجراء البزل القطني، وهو إجراء طبي يستخدم للوصول إلى السائل المحيط بالحبل الشوكي.
ومن بين المرضى الذين شاركوا في التجارب السريرية طفل يدعى أوين يبلغ من العمر 12 عاماً ويعاني من متلازمة درافيت وكانت نوباته لا تستجيب للعلاج الدوائي، كما كان يعاني أيضاً من إعاقة ذهنية وصعوبات في المشي. وبعد تلقي العلاج الجديد انخفضت نوبات الصرع لديه بشكل ملحوظ كما تحسنت قدراته اللغوية وسلوكه بشكل واضح، بحسب الدكتورة لوكس.
وقالت والدته إن التغيير كان كبيراً في حياة طفلها إذ أصبح قادراً على تكوين صداقات، وهو أمر جديد تماماً بالنسبة له، وأضافت: "جودة حياته تحسنت بشكل كبير لدرجة أنه أصبح قادراً على الاستمتاع بالمزيد من الأنشطة مع الأطفال الآخرين".
وشملت التجربتان السريريتان، اللتان أجريتا في عدة مراكز طبية بالولايات المتحدة والمملكة المتحدة، 81 مريضاً تتراوح أعمارهم بين عامين و18 عاماً كانوا يتلقون بالفعل أدوية تقليدية مضادة للصرع.
وأظهرت النتائج أن المرضى الذين تلقوا جرعتين إلى 3 جرعات بتركيز 70 ملليجرام من الدواء شهدوا انخفاضاً في نوبات الصرع الحركية بنسبة تقارب 85٪ بعد 3 أشهر من العلاج، و73٪ بعد 6 أشهر.
البزل القطني
بعد انتهاء المرحلة الأولى من الدراسة انتقل المرضى المؤهلون إلى مرحلة متابعة مفتوحة وتلقوا جرعة مقدارها 45 ملليجرام من الدواء كل 4 أشهر.
وخلال أول 20 شهراً من المتابعة استمرت نسبة انخفاض النوبات بين 58 و90٪. أما المرضى الذين استمروا في هذه المرحلة لأكثر من 36 شهراً فقد أظهروا تحسناً ملحوظاً في مهارات التواصل التعبيري والاستقبالي.
ورغم أن معظم المرضى تعرضوا لآثار جانبية مرتبطة بالعلاج، فإن الغالبية العظمى منها كانت خفيفة إلى متوسطة، وكان العرض الجانبي الأكثر شيوعاً في التجارب الأولية هو متلازمة ما بعد البزل القطني التي ظهرت لدى نحو 25٪ من المرضى.
أما في دراسات المتابعة فكان أكثر الأعراض شيوعاً هو ارتفاع مستوى البروتين في السائل الدماغي الشوكي لدى نحو 45٪ من المشاركين.
ومع ذلك لم يسجل لدى أي من هؤلاء المرضى ارتفاع في ضغط الدماغ أو حدوث استسقاء دماغي، ومن بين الآثار الجانبية الخطيرة التي ظهرت خلال الدراسة، اعتبر حدث واحد فقط مرتبط مباشرة بالعلاج.
وقالت المؤلفة المشاركة في الدراسة ليندا لوكس، إن البيانات التي جمعتها الدراسة تدعم سلامة العلاج وإمكانية تحمله لدى المرضى، إضافة إلى إظهار تحسن واضح في الحالة السريرية العامة وجودة الحياة والسلوك التكيفي لدى المرضى الذين واصلوا تلقي الجرعات في مرحلة المتابعة.
ويعمل الباحثون حالياً على تنفيذ تجربة سريرية من المرحلة الثالثة على نطاق أوسع لتقييم فعالية وسلامة علاج "زوريفونسيرسن" وهي تجربة مزدوجة التعمية تعتمد المقارنة مع علاج وهمي، وهو ما يعد الخطوة الحاسمة قبل الحصول على موافقة الجهات التنظيمية لاعتماد العلاج للاستخدام الطبي.
وتشكل هذه النتائج خطوة مهمة في مجال الطب الجيني الذي يسعى إلى علاج الأمراض الوراثية من خلال استهداف أسبابها الجزيئية المباشرة، وهو اتجاه متنام في أبحاث الأعصاب والطب الدقيق.