كشفت دراسة علمية حديثة أجراها باحثون من تايوان والمملكة المتحدة عن دور جيني جديد قد يفسر أحد أكثر أشكال الصرع تعقيداً ومقاومة للعلاج.
وأظهرت النتائج أن طفرات في جين يُعرف باسم FOXJ3 ترتبط بظهور الصرع البؤري المقاوم للأدوية، وهو نمط من الصرع غالباً ما يكون مصحوباً بتشوّه بنيوي في قشرة الدماغ يُعرف بـ"خلل التنسج القشري البؤري".
وبحسب الدراسة المنشورة في دورية Nature Communications، يعمل هذا الجين كمُنظّم رئيسي لعملية تشكّل طبقات القشرة الدماغية خلال المراحل المبكرة من التطور. وعندما يختل عمله، يؤدي ذلك إلى اضطراب في بناء هذه الطبقات، ما يخلق بيئة عصبية مهيّأة لحدوث نوبات صرع لا تستجيب للعلاجات الدوائية التقليدية.
ويُعدّ خلل التنسج القشري البؤري اضطراباً نمائياً ينشأ قبل الولادة، نتيجة تشكّل غير طبيعي لطبقات القشرة الدماغية، ما يؤدي إلى توزيع غير منتظم للخلايا العصبية في مناطق محددة من الدماغ، وهو ما يرتبط بحدوث نوبات صرع متكررة غالباً ما تكون مستعصية على العلاج.
التنسج القشري البؤري
تتألف القشرة الدماغية في الحالة الطبيعية من ست طبقات منتظمة من الخلايا العصبية، غير أن هذا التنظيم الدقيق يختل في حالات "خلل التنسج القشري البؤري"، نتيجة اضطراب في هجرة الخلايا العصبية خلال مراحل تطور الدماغ الجنيني، ما يؤدي إلى تموضعها في مواقع غير صحيحة أو اكتسابها أشكالاً غير طبيعية. ويترتب على هذا الخلل البنيوي نشوء بؤر كهربائية غير مستقرة داخل الدماغ، تمهد لحدوث نوبات صرع متكررة.
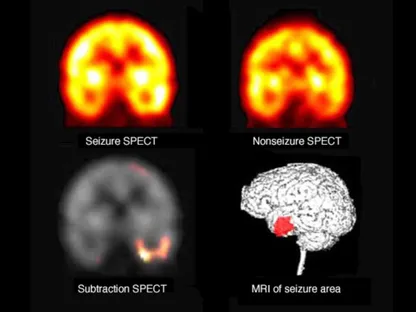
ويُعد هذا الاضطراب من أبرز الأسباب الكامنة وراء الصرع المقاوم للعلاج الدوائي، لا سيما لدى الأطفال والشباب. وبينما يمكن رصده في بعض الحالات عبر التصوير بالرنين المغناطيسي، يظل خفياً في حالات أخرى، ما يزيد من تعقيد تشخيصه.
وفي ظل فشل العلاجات الدوائية، قد يلجأ الأطباء إلى التدخل الجراحي لاستئصال المنطقة المصابة من الدماغ، شريطة أن يكون ذلك آمناً، وهو ما قد يسهم في تقليل النوبات أو القضاء عليها.
وعلى مدى السنوات الماضية، تركزت الجهود البحثية على فهم الأسس الجينية والبيولوجية لهذا الاضطراب، بهدف تطوير علاجات أكثر دقة. وفي هذا السياق، أظهرت الدراسة الحديثة أن جين FOXJ3 يؤدي دوراً محورياً في تنظيم مسار الإشارات PTEN–mTOR، وهو نظام حيوي يتحكم في نمو الخلايا وانقسامها وأيضها وبقائها.
ويعمل هذا المسار كآلية توازن دقيقة تضبط توقيت نمو الخلايا وتوقفه، وهو أمر بالغ الأهمية لضمان التطور الطبيعي للأنسجة، خصوصاً في الدماغ. وعند اختلال هذا النظام، قد تنشأ مجموعة من الاضطرابات العصبية، من بينها خلل التنسج القشري البؤري، والتصلب الحدبي، والورم الليفي العصبي.
ويرى الباحثون أن تحديد جين FOXJ3 كعامل جيني جديد ضمن الأمراض المرتبطة بخلل مسار mTOR يُمثّل خطوة متقدمة نحو فهم الجذور البيولوجية للصرع وتشوهات القشرة الدماغية، كما يفتح آفاقاً واعدة لتطوير علاجات تستهدف هذه المسارات الجزيئية بدقة أكبر.
وبدأت خيوط هذه الدراسة عندما تمكَّن الباحث يو-تسن ليو من تشخيص حالة عائلية تعاني من صرع مقاوم للأدوية مرتبط بخلل التنسج القشري البؤري، وذلك في قسم الصرع بمستشفى تايبيه لقدامى المحاربين في تايوان، ما شكل نقطة الانطلاق لهذا الاكتشاف العلمي.
تحليل الجينات
أجرى الفريق البحثي تحليلاً جينياً معمقاً لعائلات تعاني من الصرع البؤري الوراثي، بالتوازي مع تجارب مخبرية على نماذج حيوانية وخلايا مفردة، بهدف تتبّع التأثيرات الدقيقة لطفرات جين FOXJ3 على نمو الدماغ.
وكشفت النتائج أن هذه الطفرات تعطل آليات هجرة الخلايا العصبية إلى مواقعها الصحيحة خلال المراحل المبكرة من التطور، كما تؤثر لاحقاً في الأدوار الوظيفية التي تضطلع بها هذه الخلايا.
وقال المؤلف الرئيسي للدراسة، جين-وو تساي، إن خلل التنسج القشري البؤري يُعد من أكثر الأسباب شيوعاً للصرع لدى المرضى غير المستجيبين للعلاج الدوائي، إلا أن أسبابه الجذرية لا تزال غير معروفة في نسبة كبيرة من الحالات.
وأضاف تساي أن النتائج الجديدة تكشف عن حلقة جينية وجزيئية تربط بين اضطراب تطور الدماغ وظهور نوبات الصرع.
وخلال التطور الطبيعي للدماغ، تتشكل طبقات القشرة الدماغية الست وفق تسلسل دقيق يبدأ من الداخل إلى الخارج، حيث تنشأ الخلايا العصبية ثم تهاجر إلى مواقع محددة لتكوين هذه الطبقات.
وأظهرت الدراسة أن نشاط جين FOXJ3 يكون مرتفعاً في الخلايا السلفية العصبية خلال المراحل المبكرة، قبل أن ينخفض عند نقطة انتقالية حاسمة في مسار التطور. وعند اختلال وظيفة هذا الجين، تفشل الخلايا العصبية في الوصول إلى مواقعها الصحيحة، ما يؤدي إلى تراكمها في طبقات غير ملائمة داخل القشرة الدماغية.
كما بيّنت النتائج أن جين FOXJ3 ينظّم بشكل مباشر نشاط جين PTEN، الذي يُعد أحد أهم المثبطات الطبيعية لمسار mTOR، وهو مسار ارتبط سابقاً بحدوث الصرع وتشوهات الدماغ.
وعندما تعجز طفرات FOXJ3 المرتبطة بالمرض عن تنشيط PTEN، ينشط مسار mTOR بشكل مفرط، ما يؤدي إلى تكوّن خلايا عصبية كبيرة الحجم وغير طبيعية الشكل، وهي سمة مرضية شائعة في أدمغة المصابين بخلل التنسج القشري البؤري.
وأظهرت التجارب أيضاً أن إعادة تنشيط PTEN في النماذج التجريبية كانت كافية لتصحيح التشوهات القشرية، ما يشير إلى وجود محور جزيئي حاسم يربط بين FOXJ3 وPTEN ويتحكم في تطور القشرة الدماغية.
وجمعت الدراسة بين بيانات جينية لمرضى من تايوان والمملكة المتحدة، إلى جانب نتائج مستخلصة من نماذج حيوانية وتحليل الخلايا المفردة.
وأوضح الباحث يو-تسن ليو، المدير المشارك لقسم الصرع في معهد الأعصاب بمستشفى تايبيه لقدامى المحاربين، أن خلل التنسج القشري البؤري من النوع الثاني لا يزال السبب الأكثر شيوعاً للصرع المقاوم للأدوية، حتى لدى بعض المرضى الذين تبدو صور الرنين المغناطيسي لديهم طبيعية.
أهمية كبيرة
لا تقتصر أهمية هذه النتائج على تحديد سبب جيني جديد للصرع، بل تمتد لتوسيع الفهم العلمي للآليات التي تتحكم من خلالها الجينات في مصير الخلايا العصبية وتموضعها داخل الدماغ خلال مراحل التطور المبكر.
وعلى الصعيد السريري، تفتح هذه المعطيات آفاقاً لتحسين دقة التشخيص الجيني لدى مرضى الصرع البؤري، لا سيما أولئك الذين لا يكشف التصوير بالرنين المغناطيسي لديهم عن تشوهات واضحة، كما تمهد الطريق لتطوير علاجات موجّهة تستهدف مسار mTOR بشكل مباشر.
ويُعد الصرع من أكثر الاضطرابات العصبية انتشاراً على مستوى العالم، إذ يصيب أكثر من 50 مليون شخص، فيما لا يستجيب عدد كبير من المرضى للعلاجات المتاحة حالياً. ومن هنا، فإن فك شيفرة الأسس الجينية والتطورية للمرض يمثّل خطوة محورية نحو ابتكار استراتيجيات علاجية أكثر فاعلية.
وفي هذا السياق، أكد الباحث سانجاي إم. سيسوديا، أحد المشاركين في الدراسة، أن تحديد الآلية الجينية الدقيقة الكامنة وراء إصابة الفرد بالصرع يحمل أهمية كبيرة على المستويين الفردي والعلمي. فبالنسبة للمريض وعائلته، قد يضع هذا الفهم حداً لسنوات من البحث عن تفسير للحالة، ويوفر أساساً للاستشارات الوراثية والتخطيط الأسري.
وأضاف أن هذا الاكتشاف يفتح الباب أمام تطوير أساليب علاجية أكثر تقدماً، سواء عبر تحسين اختيار الأدوية، أو إعادة توظيف علاجات قائمة، أو حتى تطوير علاجات جينية مستقبلية، بما يمهّد لمرحلة جديدة من الإدارة الدقيقة والفعالة لهذا المرض المعقد.