كشف باحثون عن دور محوري لبروتين، يدعى RBPMS، في نمو الخلايا الجذعية اللوكيمية، وطوروا مركباً كيميائياً لتقليل نمو خلايا سرطان الدم في تجارب أولية على الفئران.
وتسلط الدراسة، المنشورة ضمن منصة الجمعية الأميركية لتقدم العلوم، الضوء على آلية جزيئية دقيقة تقف وراء عودة سرطان الدم النخاعي الحاد بعد العلاج، وتقدم هدفاً دوائياً محتملاً قد يساعد في القضاء على الخلايا المسؤولة عن الانتكاس.
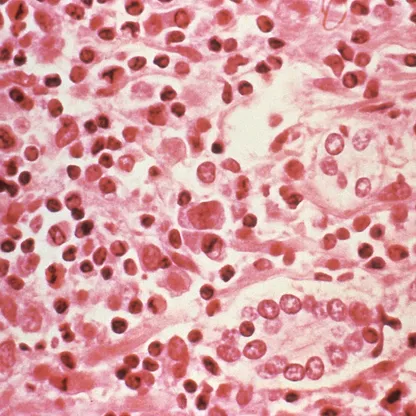
وسرطان الدم النخاعي الحاد من الأمراض التي يصعب السيطرة عليها على المدى الطويل، رغم أن كثيراً من المرضى يستجيبون للعلاج الكيميائي في البداية، لكن المشكلة تكمن في فئة صغيرة من الخلايا تعرف بـ"الخلايا الجذعية اللوكيمية"، وهي خلايا تمتلك قدرة عالية على التجدد الذاتي والبقاء.
خلايا سرطان الدم
غالباً تنجو هذه الخلايا من العلاج الأولي، لتعمل لاحقاً كبذور تعيد تكوين الورم، ما يؤدي إلى انتكاس المرض؛ لذلك، ينظر إليها على أنها الهدف الأكثر أهمية لأي علاج يسعى لتحقيق شفاء طويل الأمد.
ركز الباحثون على بروتين RBPMS، وهو بروتين يرتبط بالحمض النووي الريبي، ويعرف بوجوده في الخلايا الجذعية والخلايا الأولية، ورغم أن دراسات سابقة أشارت إلى دوره في تثبيط نمو بعض الأورام الصلبة، إلا أن دوره في سرطان الدم لم يكن واضحاً.
وأوضح الباحثون أن مستويات هذا البروتين ترتبط بشكل مباشر بشدة المرض؛ فمن خلال تحليل بيانات لبعض المرضى، وجد الباحثون أن ارتفاع تعبير RBPMS يرتبط بنتائج أسوأ وفترات بقاء أقصر.
وتشير هذه الملاحظة إلى أن البروتين لا يكتفي بالتواجد في الخلايا السرطانية، بل يلعب دوراً نشطاً في دفعها نحو سلوك أكثر عدوانية.
ولفهم الآلية، أجرى الباحثون تجارب على خلايا بشرية مزروعة ونماذج فئران، وأظهرت النتائج أن بروتين RBPMS يعمل من خلال تجنيد بروتين آخر يدعى IGF2BP3، والذي بدوره يقوم بتثبيت جزيئات الحمض النووي الريبي الخاصة بجين FOXO1.
ويلعب هذا الجين دوراً مهماً في تنظيم عمليات الأيض داخل الخلية، خاصة استهلاك الجلوكوز، ونتيجة لذلك، تحصل الخلايا الجذعية اللوكيمية على دعم أيضي يساعدها على الاستمرار في النمو والتجدد.
تقليل نمو خلايا اللوكيميا
ويعمل بروتين RBPMS كمنسق لسلسلة من التفاعلات التي تمنح الخلايا السرطانية القدرة على "تغذية نفسها" والبقاء نشطة، حتى في ظل ظروف غير مواتية مثل العلاج الكيميائي.
بعد تحديد هذا المسار، انتقل الباحثون إلى الخطوة التالية، وهي البحث عن طريقة لإيقافه، وفحصوا مكتبة كبيرة من المركبات الكيميائية، وتمكنوا من تصميم مثبط انتقائي لبروتين RBPMS، أطلقوا عليه اسم RB98.
في التجارب على الفئران، أظهر هذا المركب قدرة على تقليل نمو خلايا اللوكيميا، كما ساهم في إطالة عمر الحيوانات مقارنة بالمجموعات غير المعالجة، وتشير هذه النتائج إلى أن استهداف RBPMS قد يكون استراتيجية فعالة لكبح الخلايا الجذعية اللوكيمية.
تكمن أهمية هذه النتائج في أنها تستهدف أحد أعمق أسباب فشل العلاج، وهو بقاء الخلايا الجذعية السرطانية، فبدلاً من التركيز فقط على تقليص حجم الورم، يوجه هذا النهج العلاج نحو القضاء على "المصدر" الذي يعيد تكوينه.
كما أن تحديد آلية واضحة، تتضمن بروتينات RBPMS وIGF2BP3 وFOXO1، يوفر فهماً أدق لكيفية عمل هذه الخلايا، ما قد يساعد في تطوير علاجات أكثر دقة في المستقبل.
وأشار الباحثون إلى أن هذا النوع من الاستهداف قد يقلل من احتمالات الانتكاس، وهو أحد أكبر التحديات في علاج هذا النوع من السرطان.
رغم النتائج الواعدة، لا تزال الدراسة في مراحلها المبكرة؛ فالتجارب أجريت بشكل أساسي على نماذج حيوانية وخلايا مزروعة، ما يعني أن فعالية وسلامة المركب RB98 في البشر لم تختبر بعد.
كما أن استهداف بروتينات مرتبطة بوظائف خلوية أساسية قد يحمل مخاطر محتملة، مثل التأثير على الخلايا السليمة، وهو ما يتطلب تقييماً دقيقاً في الدراسات المستقبلية.