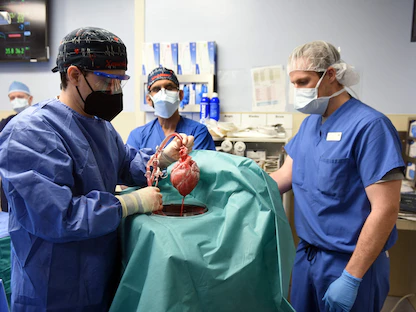
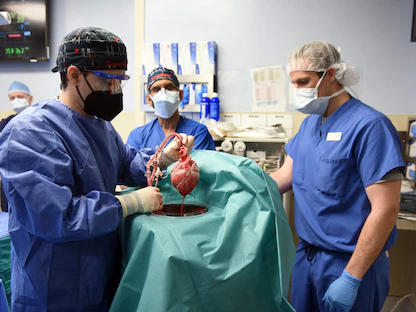
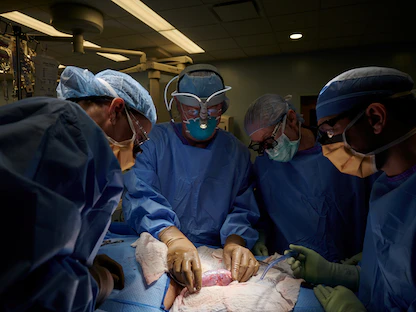
في إنجاز علمي جديد، نجح باحثون في زرع كلى من خنازير معدلة وراثياً في قرود المكاك، وأظهرت دراسة نُشرت الأربعاء، في دورية "Nature" أن عملية زرع كلى الخنازير في نموذج المكاك أبقت القرود على قيد الحياة لمدة تجاوزت 750 يوماً، مشيرةً إلى أن معدل البقاء الذي تم تحقيقه هو أكبر معدل بقاء لحيوان رئيسي تلقى كلية تم تنميتها داخل جسم خنزير.
وتُمثل هذه النتائج أكبر وأشمل مجموعة بيانات منشورة في هذا المجال حتى الآن.
تعديلات الجينوم
وتسلط الدراسة الرائدة الضوء على العديد من التعديلات التي تم إجراؤها على جينوم الخنازير، مما يوفر أدلة واعدة على أن هذه التكنولوجيا يمكن أن تتغلب على العقبات المناعية في المستقبل لعمليات زرع الأعضاء البشرية، وربما تُطيل بقاء هذه الأعضاء المنقذة للحياة.
ومنذ السبعينات والثمانينات أصبحت زراعة الأعضاء البشرية من متبرع إلى متلقي علاج، أمراً مقبولاً، لكن توفر الأعضاء مقارنة بالاحتياجات لا يزال قليلاً للغاية، إذ إن معظم الأفراد المصابين بخلل الأعضاء في المرحلة النهائية يموتون في انتظار عضو متبرع مناسب.
ويمكن لزراعة الأعضاء الحيوانية في البشر أن تتغلب على هذا العجز، وتنقذ العديد من الأرواح البشرية.
لماذا الخنازير؟
تعد الخنازير أكثر الحيوانات المانحة الواعدة، وذلك بسبب توفر التكنولوجيا اللازمة لتعديل الجينوم الخاص بها، وقصر فترة حملها، ونموها السريع إلى حجم متوافق مع الإنسان، والتشابه التشريحي لأعضائها مع أعضاء البشر، لكن التغلب على رفض أعضاء الخنازير من قبل الجهاز المناعي البشري شكل تحدياً لأكثر من 40 عاماً.
وفي السنوات القليلة الماضية، أدت تكنولوجيا تحرير الجينات المحسنة (تقنية كريسبر) والعلاجات المثبطة للمناعة إلى تشجيع تجارب البقاء على قيد الحياة باستخدام عضو حيواني.
وفي يناير 2022، تم إجراء أول عملية زرع قلب من خنزير إلى إنسان، إلا أن المريض توفي بعد شهرين فقط من زراعة ذلك القلب.
ومنعت التعديلات الوراثية التي أجراها الباحثون على الخنازير رفض العضو المزروع، وأطالت بقاء القرود على قيد الحياة لمدة تتجاوز عامين.
وتنتمي قرود المكاك للرئيسيات، وهي رتبة من طائفة الثدييات ينتمي إليها الإنسان أيضاً، وهذا يعني وجود تشابهات ضخمة بين الإنسان وقرود المكاك من الناحية البيولوجية والتشريحية، وهو الأمر الذي يُعزز فكرة نجاح الأعضاء المزروعة من الخنازير في البشر.
أسباب رفض الأعضاء
في حديث لـ"الشرق"، قال المؤلف المشارك في الدراسة مايكل كيرتس إن الدراسة تضمنت 3 تعديلات وراثية مهمة لكلى الخنازير، تمثّلت في إزالة 3 جينات مسؤولة عن تخليق مستضدات الجليكان، والتي كانت متورطة في الرفض المفرط الحدة للأعضاء.
ومستضدات الجليكان هي جزيئات تتكون من الكربوهيدرات (سلاسل السكر أو الجليكان) التي يمكن أن تؤدي إلى استجابة مناعية في الجسم، وهي نوع من المستضدات التي يتعرف عليها الجهاز المناعي، وتحديداً عن طريق الأجسام المضادة. وتلعب تلك المستضدات دوراً حاسماً في العمليات البيولوجية المختلفة، بما في ذلك الاستجابات المناعية والتعرف على الخلايا الخلوية.
ويمكن العثور على مستضدات الجليكان على سطح الخلايا، بما في ذلك خلايا الأعضاء المزروعة. وعندما يتم التعرف على هذه المستضدات الجليكانية على أنها غريبة من قبل الجهاز المناعي للمتلقي، فإنها يمكن أن تؤدي إلى استجابة مناعية تؤدي إلى رفض العضو.
وبإزالة تلك المستضدات، تغلّب الباحثون على عائق رئيسي يحول دون عملية زرع الأعضاء من الحيوانات.
جينات بشرية متحورة
قال كيرتس إنه تم إدخال 7 جينات بشرية محورة في جينات الخنازير بهدف تنظيم مسارات متعددة تُعدل الرفض، بما في ذلك الالتهاب، والمناعة الفطرية، والتخثر، والمكملات.
كما قام الفريق بتعطيل الفيروسات التقهقرية داخلية المنشأ الموجودة في جينوم الخنازير، مما يُعزز التوافق بشكل أكبر.
وللمقارنة، أظهرت الكلى التي لم تُعدل وراثياً، واحتوت على مستضد الجليكان ضعفاً في البقاء على قيد الحياة، في حين أن الكلى التي جرى تعديلها أظهرت مدة أطول 7 مرات، بمتوسط 24 يوماً مقابل 176 يوماً، على التوالي.
وأكد هذا الاختلاف المذهل على الإمكانات الهائلة للتعبير عن الجينات البشرية في ترقيع كلى الخنازير لضمان البقاء على المدى الطويل.
ونجحت الكلى المانحة التي تحمل الجينات المحورة البشرية والمهندسة وراثياً إلى فترات بقاء أطول بشكل ملحوظ عند زراعتها في قرود المكاك.
وكشف التحليل الوظيفي في المختبر أن الخلايا البطانية المعدلة لكلية الخنازير عدلت الالتهاب بطريقة تشبه إلى حد كبير الخلايا البطانية البشرية، مما يُشير إلى مستوى عالٍ من التوافق المناعي البشري في الخلايا المعدلة جينياً.
وعلاوة على ذلك، أظهر تقييم المؤشرات الحيوية لوظيفة الكلى لدى المتلقين من القرود أن كلية خنزيرية مزروعة واحدة قامت بتصفية السموم بكفاءة، مما يعوض عن عدم وجود كليتين أصليتين.
وأوضحت المؤلفة المشاركة في الدراسة وينج كوين خلال مؤتمر صحافي الثلاثاء، أن الدراسة نجحت في إيقاف الأجسام المضادة الموجودة مسبقاً، سواء كانت بشرية أو غير بشرية من التفاعل مع جزيئات الخنازير التي تسبب رفض الكلى المزروعة.
السلامة والمخاوف الأخلاقية
لكن، ماذا عن إجراءات السلامة حال استخدام كلى تم تنميتها داخل خنزير وزراعتها داخل البشر؟
في رده على سؤال لـ"الشرق"، أشار كيرتس إلى أن الفريق ناقش مع إدارة الغذاء والدواء في الولايات المتحدة إجراءات السلامة بشكل جدي ومتواصل.
وأضاف أن أحد المخاوف الأساسية المتعلقة بالسلامة في زراعة الأعضاء هو احتمالية أن يتعرف الجهاز المناعي لدى المتلقي البشري على عضو الخنزير باعتباره عضواً غريباً، ويقوم باستجابة مناعية، مما يؤدي إلى رفض العضو، وتابع "نجحنا في تلافي تلك المشكلة عن طريق حذف وتعديل المستضدات الموجودة على سطح خلايا الخنازير، والتي تؤدي إلى هذه الاستجابات المناعية".
كما تنطوي عملية زراعة الأعضاء من الخنازير على خطر نقل العدوى أو الأمراض الحيوانية المنشأ من الخنازير إلى البشر، ويشمل هذا الخطر الفيروسات التقهقرية، ومسببات الأمراض المحتملة الأخرى، وبشأن ذلك لفت كيرتس إلى أن "تلك المسألة تمت معالجتها بالفعل عن طريق تعطيل الفيروسات التقهقرية المنشأ".
وتُقدم الدراسة أيضاً نتائج طويلة المدى وبيانات يصفها كيرتس بـ"الصلبة"، ما سيُساعد على إجراء التجارب على البشر في غضون عامين اثنين من الآن، وفق قوله.
"قضية أخلاقية"
عملية زراعة أعضاء الخنازير في البشر تُثير مجموعة من القضايا الأخلاقية التي يجب النظر إليها بعناية، وتشمل هذه المخاوف مجموعة واسعة من المواضيع، بما في ذلك رعاية الحيوان، والموافقة المستنيرة، والمخاطر المحتملة، والآثار الاجتماعية الأوسع.
فاستخدام الحيوانات، وخاصة الخنازير، كمتبرعين بالأعضاء، يُثير مخاوف أخلاقية بشأن علاج ورفاهية هذه الحيوانات. ويمكن اعتبار التعديل الوراثي وتربية الحيوانات لغرض وحيد هو توفير الأعضاء اللازمة لزراعة الأعضاء البشرية بمثابة مشكلة أخلاقية، وتشمل الاعتبارات الأخلاقية الظروف التي يتم فيها تربية هذه الحيوانات، وما إذا كانت ستواجه معاناة غير ضرورية.
وفي سياق زراعة الأعضاء السريرية، يُعد الحصول على موافقة مستنيرة من المرضى أمراً ضرورياً، إذ يجب على المرضى أن يفهموا تماماً المخاطر المحتملة والشكوك والآثار طويلة المدى لتلقي عضو من مصدر حيواني، كما أن هناك حاجة لتقييم مخاطر وفوائد زراعة الأعضاء بعناية، مثل انتقال الأمراض الحيوانية المنشأ، وضرورة تثبيط المناعة على المدى الطويل.
وقال كيرتس تعليقاً على ذلك الأمر إن المخاوف الأخلاقية أمر لا يُمكن الاستهانة به على الإطلاق، مشيراً إلى أنها ستخضع لمناقشة موسعة قبل بدء التجارب على البشر.